Eschborn – Eine orale Substitution mit Verdauungsenzymen zu den Mahlzeiten ist die einzige Möglichkeit zur Therapie der exokrinen Pankreasinsuffizienz (EPI)1, einer Störung der Verdauungsenzymproduktion des Pankreas. Die hierzu eingesetzten Lipasen unterscheiden sich in ihrer Effizienz. So zeigte in einer aktuellen in vitro-Studie2 die Rizolipase aus Reispilzen eine vergleichbar hohe Spaltaktivität wie die porzine Lipase bei einem physiologischen pH-Wert von 7 (58 % versus 57 %), aber eine höhere Aktivität bei niedrigeren Werten (pH 3-4). Auch die Spaltaktivität unter physiologischen Gallensalzkonzentrationen war für die Rizolipase mit 69 % höher als bei der porzinen Lipase mit 58 %. Individuelle Milieubedingungen im Gastrointestinaltrakt, wie eine erhöhte Säurelast im Duodenum oder die Menge an Fett-emulgierenden Gallensalzen, sind eine therapeutische Herausforderung, die den Erfolg einer Substitution beeinflussen. „Die natürliche Säurestabilität der Rizoenzyme ist eine wesentliche Grundlage für ihre gute Wirksamkeit, z. B. bei Pankreatin Non-Respondern. Einem Therapieversagen aufgrund einer Übersäuerung des GI-Traktes bei Bicarbonatmangel oder nach Operationen am Verdauungstrakt kann so entgegengewirkt werden“, bringt Prof. Ahmed Madisch die Ergebnisse der Studie mit seinen Erfahrungen aus der klinischen Praxis in Einklang.
Bei einer EPI ist die Produktion aller Verdauungsenzyme des Pankreas, vor allem aber der Lipase gestört. Die Fettverdauung kann nur unzureichend erfolgen und resultiert in postprandialen Diarrhoen, Steatorrhoen, subjektiver Fettunverträglichkeit, quantitativer und qualitativer Malnutrition mit Resorptionsstörungen für fettlösliche Vitamine und Mineralstoffe. Die aktuelle in vitro-Studie vergleicht die Wirksamkeit zweier Lipasen aus zur Therapie der EPI zugelassenen Arzneimitteln: porzine Lipase aus Schweinepankreas (Pankreatin) und Lipase aus Reispilzen (Rizolipase, in NORTASE®). Gemessen wurde die lipolytische Aktivität der homogenisierten Pankreatinpellets und des Rizoenzympulvers als Freisetzung von freien Fettsäuren aus Olivenöl im Verhältnis zur Kontrolle unter verschiedenen physiologischen und pathologischen Bedingungen.
Rizolipase unbeeinflusst von der Säurelast
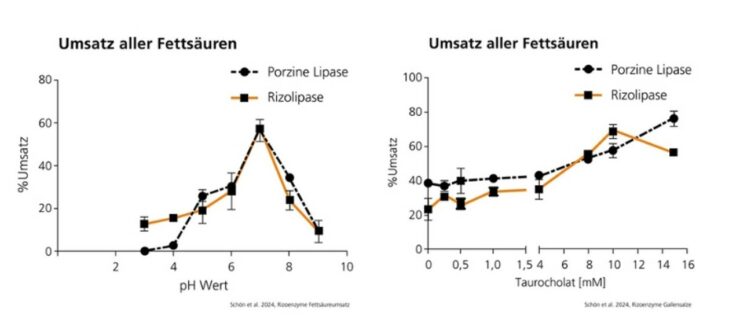
Bei nicht zufriedenstellender Symptomreduktion mit Pankreatin wird die zusätzliche Gabe von Protonenpumpenhemmern bzw. Bicarbonat empfohlen3,4, was sich oft auf eine herabgesetzte Pankreatinaktivität (Denaturierung) durch eine erhöhte Säurelast zurückführen lässt. Aus diesem Grund wurde in dieser in vitro-Untersuchung die Aktivität der Lipasen bei physiologisch als auch pathologisch erreichbaren pH-Werten des Gastrointestinaltrakts (pH 3-9) untersucht. Die maximale Spalteffizienz (57 % Pankreatin, 58 % Rizolipase) erreichten die auf die gleichen Enzymeinheiten standardisierten Lipasen bei pH 7, dem physiologischen pH-Wert des Duodenums. Während Rizoenzyme bereits bei pH 3-4 alle untersuchten Fettsäuren effektiv spalten (Abb. 1a) und beispielsweise bei der Ölsäure (Hauptkomponente des Olivenöls) einen Umsatz von 73 % zeigten, war die porzine Lipase erst ab einem pH-Wert von 5 aktiv. In Patienten setzt der galenische Säureschutz der Pankreatinpellets die Lipase jedoch erst bei höheren pH-Werten im Duodenum frei5.
Relevanz säureaktiver Verdauungsenzyme
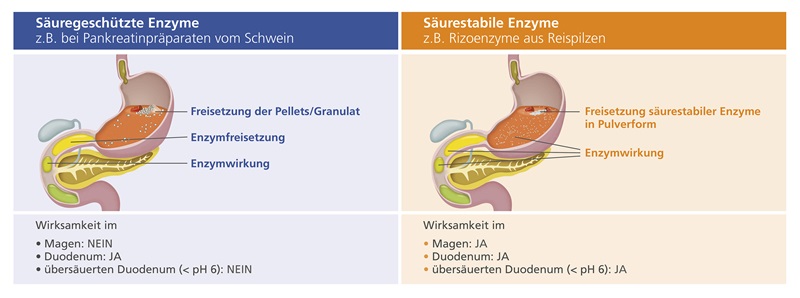
Das breite pH-Spektrum von pH 3-96,7 erlaubt den Rizoenzymen eine effektive Lipolyse direkt nach Öffnung der Kapsel im postprandial sauren Gastrum (pH 3-5)8 als auch im neutralen oder übersäuerten Duodenum. „Durch das erweiterte Wirkzeitfenster der Rizolipase wird ein Teil der Fettverdauung bereits im Magen erreicht, die mit porzinen Lipasen auf das pH-neutrale Duodenum beschränkt ist“, so der Gastroenterologe aus Frankfurt. Relevant wird diese Eigenschaft, wenn mit zunehmender Schwere der EPI auch die Produktion des Chymus neutralisierenden pankreatischen Bicarbonats reduziert ist9-12. Auch Pylorusdefekte, kurze Magentransitzeiten bzw. Dumping (wie z. B. bei Diabetes und Cystischer Fibrose, Karzinome, chirurgische Eingriffe am Pankreas) führen zu unphysiologischer Ansäuerung des Duodenums. Die säureaktiven Rizoenzyme machen auch den Einsatz von Protonenpumpenhemmern überflüssig, deren Langzeitanwendung zu unerwünschten Effekten führen kann13.
Die frühe Fett- und Proteinverdauung durch Rizoenzyme im Gastrum kann zudem die Zellen des Duodenums zur Produktion der Signalmoleküle CCK, Sekretin und Gastrin triggern und so bei vorhandener Restaktivität des Pankreas schon früh die Freisetzung von Verdauungsenzymen und Bicarbonat initiieren. Bedeutsam wird dies vor allem bei Whipple OPs, bei der die Signaltransduktion durch Teilresektionen der Verdauungsorgane erschwert ist. „Durch die vorzeitige gastrale Vorverdauung und die daraus resultierenden Signalstoffe wird auch das Inkretinsystem positiv beeinflusst, wodurch beispielsweise die Insulinproduktion geregelt wird“, erläutert Madisch.
Einfluss von Gallensalzen auf die Lipolyse
Wesentlich für die Spaltaktivität der porzinen Lipase und Rizolipasen im Duodenum ist die Anwesenheit von Gallensalzen, die das Nahrungsfett emulgieren (Triglyceridmizellen). Die Aktivität der porzinen Lipase (gemessen bei pH 7) steigt in vorliegender Studie mit steigenden Gallensalzkonzentrationen (Taurocholat) im physiologischen Bereich von 0 bis 10 mM14 um
Faktor 2, die der Rizolipase um Faktor 2,9. Die Freisetzungsrate aller gemessenen Fettsäuren bei 10 mM war für die Rizolipase mit 69 % höher als bei Pankreatin mit 58 % (Abb. 1b). Nur bei pathologisch hohen Gallensalzkonzentrationen ab 16 mM war ihre Umwandlungsrate etwas niedriger als bei Pankreatin, jedoch immer noch höher als bei niedrigen Gallensalzkonzentrationen. Bei Patienten mit schwerer EPI sind eher niedrigere Gallensalzkonzentrationen im Bereich von 4 mM zu erwarten12,15. Ein inhibitorischer Effekt der Gallensalze auf die Effektivität oder gar eine Inaktivierung konnte bei beiden Präparaten nicht festgestellt werden. „Die hohe Aktivität der Rizoenzyme in der Studie deckt sich auch mit den klinischen Erfolgen. Immer häufiger werden die vegetarischen Rizoenzyme als Alternative zu tierischem Pankreatin eingesetzt“, betont der Gastroenterologe.
Diese und weitere Abbildungen sowie die Quellenangaben sind über den Pressekontakt erhältlich.
Pflichttext
NORTASE®
Anwendungsgebiete: Störungen der exokrinen Pankreasfunktion, die mit einer Maldigestion einhergehen. Zusammensetzung: 1 Hartkapsel enthält: Rizolipase (Lipase aus Rhizopus oryzae) entspr. 7.000 FIP-E., Protease aus Aspergillus oryzae mind. 54 FIP-E., Amylase aus Aspergillus oryzae mind. 700 FIP-E.. Sonstige Bestandteile: Hydroxypropylmethylcellulose (HPMC), Lactose-Monohydrat, Magnesiumstearat, Farbstoffe: Titandioxid E 171, Eisen(III)-oxid E 172. Enthält Lactose. Gegenanzeigen: Akute Pankreatitis, akuter Schub einer chronischen Pankreatitis, bekannte Überempfindlichkeit gegen Schimmelpilze (Schimmelpilzallergie) oder einen der sonstigen Bestandteile. Nebenwirkungen: Selten: unspezifische Begleiterscheinungen wie Diarrhoe, Übelkeit, Obstipation und Oberbauchbeschwerden sowie allergisch bedingte Atem- und Hautreaktionen nach berufsbedingter Sensibilisierung mit Schimmelpilzenzymen. Pharmazeutischer Unternehmer: Repha GmbH Biologische Arzneimittel, Alt-Godshorn 87, 30855 Langenhagen. Stand 03/21.
Redaktioneller Hinweis zur geschlechtsneutralen Formulierung: Ausschließlich zur besseren Lesbarkeit wird in dieser Pressemeldung auf die geschlechtsspezifische Schreibweise verzichtet. Alle personenbezogenen Formulierungen in diesem Text sind somit geschlechtsneutral zu interpretieren.